藥物設計的主要亮點
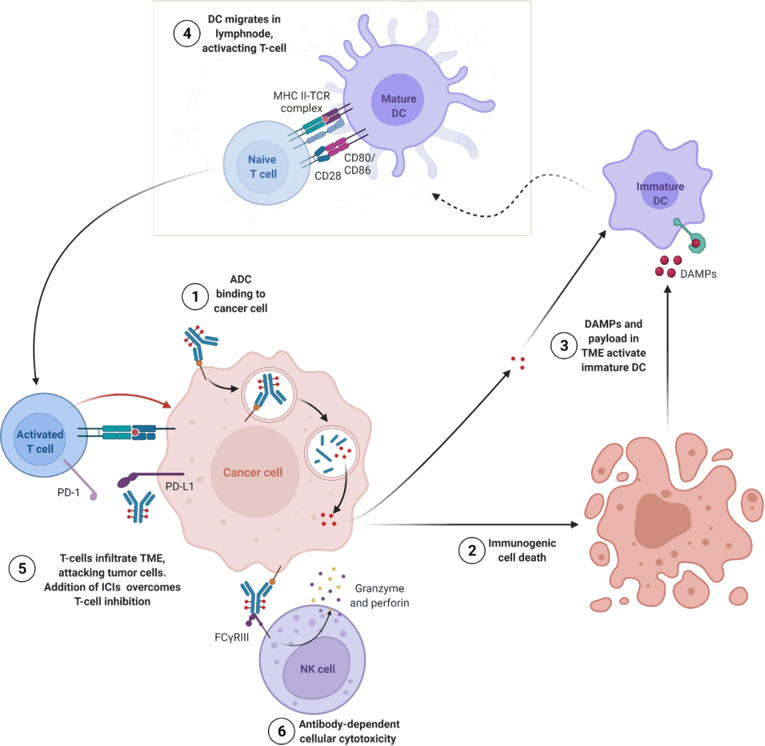
經過驗證的機製,擁有差異化的分子設計
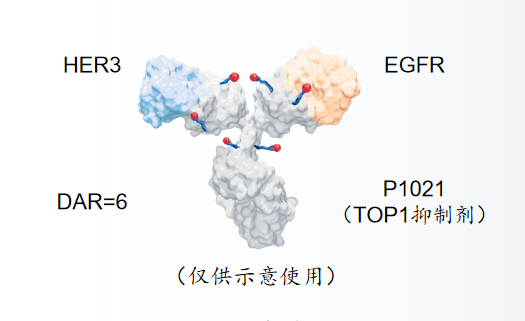
・差異化「1+1」形式設計
・在EGFR耐藥、EGFR低表達或HER3耐藥模型中展現出更佳療效
・與傳統的單特異性ADC相比,提高了治療效果
基於對生物學深刻理解的獨特設計
・對腫瘤細胞的結合親和能力高於健康細胞
・更好的內吞性,增強對腫瘤的有效載荷
各種設計策略
・TAA+I0(DB-1419)-同時靶向(i)腫瘤細胞上的TAA,以誘導腫瘤細胞死亡;及(ii)10抗原,以利用免疫系統實現協同效果
・TAA+TAA(DB-1418)-靶向兩種不同且經優化選擇的TAA.該等TAA在相同的癌細胞中共同表達,以改善抗腫瘤療效,並降低脫靶毒性